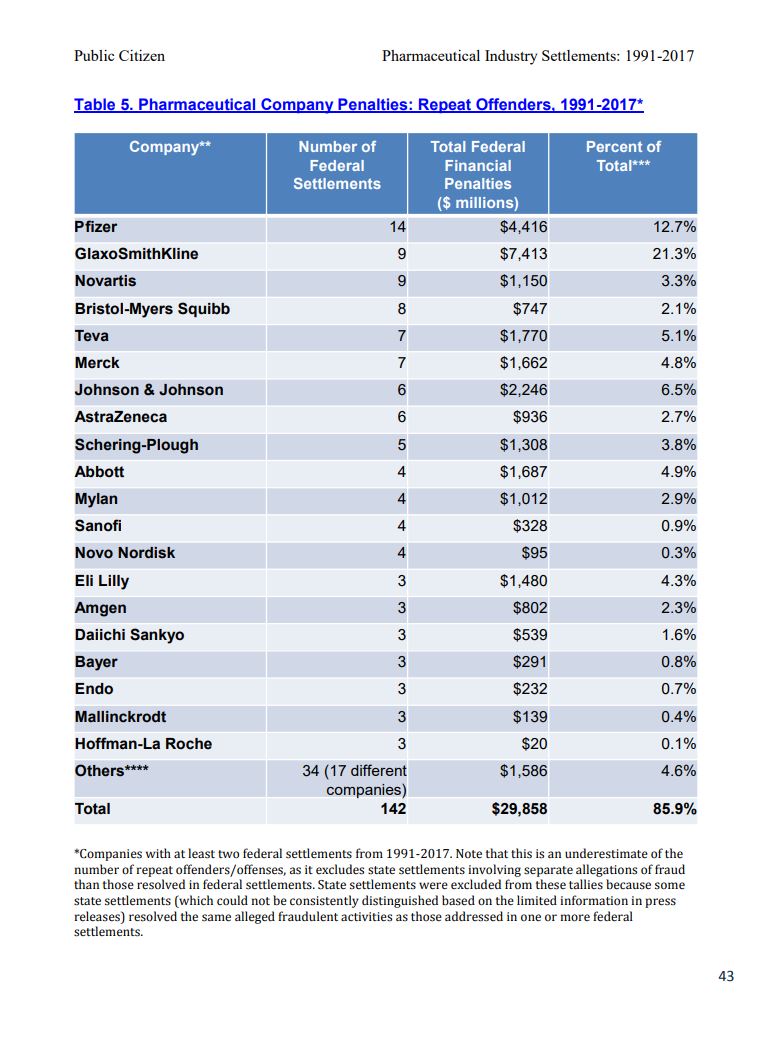
C’est carrément lunaire, comment est-il possible d’écrire autant d’âneries sans rougir de honte ? Vous avez donc cette interview d’une des responsables de Pfizer, ITW réalisée par le cabinet de conseil McKinsey ! Il s’agit donc du cabinet de conseil qui a été condamné dans le scandale des opioïdes de synthèse aux USA à une amende de 573 millions de dollars il y a à peine un an, qui va interviewer un des laboratoires pharmaceutiques les plus condamné par la justice ! On croit rêver ! Pfizer est certainement un des laboratoires, si ce n’est Le laboratoire, qui personnifie les dérives criminelles de Big Pharma. Vous pouvez lire le nombre incalculable de condamnation que Pfizer cumule entre 1991 et 2017 dans le rapport réalisé par Public Citizen.
Il ne vous reste plus qu’à lire les réponses de Angela Hwang, le texte en rouge ci-dessous, pour vous rendre compte de la gravité de la situation et du degré de déconnexion totale de cette femme avec le monde réel, notamment les décisions judiciaires produites par les tribunaux US.
Cette interview fait partie des vaccins « COVID-19 : The road to recovery and beyond », une série qui présente un large éventail de voix menant l’effort mondial historique pour développer, distribuer et fournir un accès équitable aux vaccins COVID-19, y compris les CDC africains, CEPI, Gavi, l’Alliance du Vaccin, Moderna et Pfizer.
La pandémie de COVID-19 continue d’avoir un impact dévastateur dans le monde entier. Et Pfizer, une marque pharmaceutique mondiale, s’avère être l’un de ses redoutables adversaires. Le fabricant de médicaments, qui a 172 ans, exploite toutes ses capacités et ses ressources pour réduire les risques de la COVID-19, ce qui le place à l’avant-garde de la création de vaccins. Il s’est associé à BioNTech, une société de biotechnologie basée en Allemagne, pour mettre à la disposition de milliards de personnes dans le monde le premier vaccin en son genre basé sur l’ARN messager (ARNm). Les sociétés ont augmenté leurs prévisions de fabrication de médicaments, visant à produire trois milliards de doses de vaccin COVID-19 en 2021 et quatre milliards en 2022.1 Avec environ 80 000 employés et une culture forte et contraignante, Pfizer ajoute également une dimension humaine à la lutte contre l’une des crises sanitaires les plus complexes que le monde ait jamais connues.
Angela Hwang, présidente de groupe de Pfizer Biopharmaceuticals, estime que l’histoire de Pfizer l’a aidé à se placer en première ligne des percées scientifiques liées au COVID-19. Mais il n’y a pas que la science qui compte : elle explique comment les racines profondes de Pfizer et la confiance qu’elle a en elle-même lui ont permis de devenir une force majeure dans la lutte contre les contraintes de l’approvisionnement mondial en vaccins.
En décembre 2020, un partenariat entre Pfizer et BioNTech (Pfizer-BioNTech) a produit l’un des premiers vaccins COVID-19 à recevoir une autorisation d’utilisation d’urgence (EUA) de la Food and Drug Administration (FDA) américaine pour les personnes âgées de 16 ans et plus. Elle a ensuite été étendue aux adolescents de 12 à 15 ans. En août 2021, le vaccin COVID-19 de Pfizer-BioNTech a reçu l’approbation complète de la FDA pour être utilisé dans le groupe d’âge des 16 ans et plus.2 Les efforts de R&D en matière de vaccins se concentrent désormais sur les questions critiques de récupération, telles que les souches variantes, ainsi que sur le besoin potentiel futur et l’accessibilité des rappels. “Ce programme de vaccination nous a beaucoup appris sur les domaines où le temps est dépensé et ceux où il peut être raccourci. Je suis persuadé que nous allons tous progresser du point de vue du développement et que nous aurons une idée encore plus claire des points d’accélération possibles”, déclare M. Hwang.
Le dirigeant de Pfizer s’est entretenu avec David Quigley, associé principal de McKinsey, sur la manière dont l’entreprise a été en mesure de s’adapter rapidement à la lutte contre le COVID-19, sur le rôle que les injections de rappel pourraient jouer dans la reprise mondiale et sur les raisons pour lesquelles Pfizer pense que l’exploitation de l’esprit humain est un ingrédient nécessaire à la réussite. Ce qui suit est un extrait édité de leur conversation.
McKinsey : Pfizer est l’une des plus anciennes et des plus grandes entreprises pharmaceutiques du monde. Quels éléments de la culture et de l’organisation de Pfizer lui ont permis de répondre rapidement à la crise du COVID-19 ?
Angela Hwang : La première chose que nous avons dû reconnaître est que nous étions dans une pandémie et que le temps ne jouait pas en notre faveur. Lorsque les taux d’infection ont commencé à augmenter, nous savions que si nous voulions avoir un impact quelconque, nous devions créer un vaccin en un temps record. Ce contexte a suralimenté notre état d’esprit, nos niveaux d’énergie, ainsi que notre résilience et notre détermination à résoudre le problème. Lorsque vous savez qu’il n’y a pas de temps à perdre, votre niveau de créativité, de rapidité et de prise de décision s’en trouve nettement amélioré.
Ce fut un voyage extraordinaire, motivé par l’objectif que nous avions tous, à savoir que le monde, y compris nous-mêmes et nos familles, avait besoin d’un vaccin. Lorsque vous êtes confronté à quelque chose comme ça, tout d’un coup, vous vous surprenez vous-même avec ce que vous pouvez faire.
Mais nous avons aussi eu nos moments de doute, avec des questions comme “Pouvons-nous vraiment le faire ? Pouvons-nous le faire ?” Nous nous sommes attachés à faire en sorte que l’ensemble de l’entreprise croie en elle-même : que le développement de ce vaccin, à ce rythme, au volume requis – et tout cela en respectant les normes élevées de Pfizer en matière de qualité et de sécurité – était réellement possible. Nous nous sommes donc efforcés d’amener nos employés – et nous-mêmes – à y croire.
Le travail d’équipe s’ensuit : avoir un objectif commun, partager les informations, être sur la même longueur d’onde et faire le prochain pas ensemble. Si vous voulez faire quelque chose d’aussi massif, vous ne pouvez pas être divisés. Il n’y a qu’un seul objectif et une seule façon de l’atteindre. Le travail d’équipe et la confiance étaient des éléments essentiels pour pouvoir avancer au rythme requis. Il a toujours fait partie de notre culture qu’avec des niveaux élevés de confiance, vous vous sentez plus à l’aise pour remettre en question la pensée des autres, ce qui nous pousse tous à rechercher l’excellence et à ne jamais nous contenter d’un “assez bon”. 3
Ce qui nous a apporté un savoir-faire supplémentaire, ce sont les partenariats que nous avons établis très tôt. Malgré nos antécédents en matière de vaccins, nous n’avions jamais développé cliniquement ni commercialisé un vaccin à ARNm4 auparavant. Depuis 2018, nous travaillions avec le pionnier des ARNm, BioNTech, une société de biotechnologie de premier plan en Allemagne. Notre première collaboration était axée sur le développement d’un vaccin contre la grippe à base d’ARNm. Cette base nous a permis, à nous et à BioNTech, de commencer à travailler ensemble très tôt pour développer un vaccin contre le COVID-19, et la base de confiance et les processus établis nous ont aidés à raser chaque minute que nous pouvions trouver.
C’est la confiance, la culture et l’expertise de Pfizer, associées à la technologie et à l’innovation de BioNTech, qui nous ont permis de commercialiser ce vaccin dans des délais qui semblaient auparavant impossibles. Au total, nous avons développé et commencé à distribuer un vaccin COVID-19 en huit mois environ.
McKinsey : Comment les pratiques de leadership existantes chez Pfizer ont-elles été remises en question par la pression exercée pour fournir un vaccin à une vitesse record ?
Angela Hwang : L’un des changements de leadership les plus importants qui se sont produits concerne la prise de décision. En général, dans tout programme de développement, il y a des processus et des étapes à franchir. La gouvernance est très stricte quant à la manière dont nous passons d’une étape du développement clinique à la suivante. Sachant que nous n’avions pas beaucoup de temps, nous avons dû effacer toutes les structures de gouvernance habituelles et nous concentrer sur “ce que nous devons faire pour résoudre le problème” et mobiliser tout le monde pour le faire. Que cela ait été fait auparavant ou non, nous avons dû démanteler toutes les notions antérieures que nous avions.
Nous nous sommes réunis pratiquement tous les jours – le PDG, l’équipe de direction et les experts en la matière sur une variété de sujets – dans le seul but de partager des informations, d’être sur la même longueur d’onde et de ne quitter la pièce que lorsque des décisions étaient prises, afin de pouvoir passer à l’action suivante. Chaque jour vous présente de nouveaux problèmes que vous n’aviez pas la veille, car le monde est en constante évolution. Vous ne pouvez pas déplacer le poteau de but, donc ce flux d’informations est très important lorsque vous essayez d’avancer à des vitesses incroyables.
Cette prise de décision rapide a mis à l’épreuve nos priorités en matière de risque en termes d’investissement et d’allocation de capital. Nous n’avions pas le temps de nous préoccuper des coûts. Nous devions simplement acheter toutes les matières premières nécessaires. Nous savions que nous devions fabriquer à grande échelle, car nous n’aurions pas le temps d’effectuer les étapes typiques d’un programme traditionnel de développement de vaccins. Notre décision d’acheter des matières premières ainsi que la conception et l’ingénierie de nos unités de fabrication du vaccin comportaient des risques. Nous avons commencé à discuter d’éventuels contrats avec des pays pendant le processus de développement, avant même de disposer de données sur le vaccin. Tout devait être fait bien à l’avance, ce qui signifie que tout était à risque.
Mais lorsque l’objectif est si clair, ce qui se passe ensuite est une incroyable résolution de problèmes qui vous permet de trouver les “espaces blancs” et d’identifier ce que vous pouvez supprimer pour anticiper les obstacles potentiels. Sachant que l’étape 2 est à venir, comment s’y préparer tout en effectuant l’étape 1, de sorte que les étapes 1 et 2 se déroulent presque simultanément ?
La modification de nos objectifs et de nos méthodes de résolution des problèmes en fonction des problèmes rencontrés a probablement été la plus grande adaptation de nos pratiques de leadership au cours de ce voyage.
La modification de nos objectifs et la résolution des problèmes en fonction de la situation ont probablement été les deux plus grandes adaptations des pratiques de leadership de tout ce voyage. Car lorsque vous faites fonctionner ces deux éléments ensemble, vous vous étonnerez vous-même et vos équipes de ce que vous pouvez faire, même dans les moments les plus sombres.
McKinsey : Le vaccin Pfizer-BioNTech est le premier à recevoir l’EUA américaine pour les adolescents âgés de 12 à 15 ans. Quelles sont les prochaines étapes pour faire face à la menace permanente du COVID-19 ?
Angela Hwang : Notre programme de vaccination contre le COVID-19 se veut complet et solide. Pour prendre l’exemple des 12-15 ans, cette tranche d’âge est essentielle car nous envisageons d’étendre nos vaccinations à des personnes de plus en plus jeunes. En mars 2021, nous avons commencé à étudier le vaccin chez les enfants âgés de six mois à 11 ans.
Un travail considérable est également en cours concernant la formulation du vaccin proprement dit. La forme liquide congelée était ce que nous devions utiliser pour sortir rapidement du lot. Mais pour atteindre le plus grand nombre de personnes possible, nous devons continuer à trouver des moyens de simplifier le vaccin et ses conditions de stockage. D’autres questions auxquelles nous devons répondre concernent la durabilité du vaccin.
Ensuite, il y a notre travail sur les variantes. Il y a deux voies à envisager. La première consiste à comprendre si le vaccin actuel sera suffisant pour protéger contre le COVID-19 causé par les variants qui apparaissent. C’est donc une piste de réflexion. En même temps, nous évaluons également le besoin potentiel d’un nouveau vaccin ou d’une mise à jour du vaccin avec un ARNm différent pour correspondre, par exemple, à la protéine de pointe d’une variante qui a échappé à la protection du vaccin actuel. À quoi cela ressemblerait-il ?
La bonne nouvelle, c’est que nous réfléchissons à toutes ces questions et que des essais sont en cours. Lorsque je parle de ce sujet, on me demande souvent : “Si vous devez fabriquer un nouveau vaccin ou un vaccin actualisé, combien de temps cela prendra-t-il ? Est-ce que cela nous prendra à nouveau une année entière ?” Nous ne le pensons pas. C’est là toute la beauté de la technologie de l’ARNm. Selon nos estimations – en fonction du processus réglementaire – nous serions en mesure de développer un nouveau vaccin ou une mise à jour d’un vaccin en une centaine de jours. Nous avons l’esprit tranquille, car nous savons que nous disposons probablement des outils dont nous avons besoin pour nous attaquer au virus du point de vue du développement d’un vaccin, alors qu’il continue à évoluer et à se déplacer dans le monde.
McKinsey : Que signifie, selon vous, le rythme actuel de l’innovation pour le développement de vaccins autres que ceux destinés au COVID-19 ? Comment le développement de médicaments en général pourrait-il être affecté ?
Angela Hwang : Notre nouveau monde n’est pas celui dans lequel nous vivions, même pas il y a un an. La pandémie de COVID-19 nous a profondément changés à bien des égards, que ce soit au travail ou à la maison. Bon nombre des leçons que nous avons tirées de ce périple en matière de développement de médicaments sont reproductibles. Par exemple, lorsque vous recrutez pour vos essais cliniques, il y a des processus et des activités standard à suivre. Pendant la pandémie, nous avons appris à utiliser les journaux électroniques des patients afin que les données relatives aux patients puissent être recueillies instantanément, ce qui nous a permis de gagner en efficacité dans nos études cliniques et nos interactions avec les autorités réglementaires. Je pense que des processus efficaces et basés sur la technologie comme ceux-ci resteront en place.
Autre mesure proactive, tous nos sites d’essais cliniques ont été mobilisés pendant que les protocoles étaient examinés par la FDA. Je me souviens de l’après-midi où la FDA a approuvé notre protocole de phase III : dans les deux heures qui ont suivi, nous avons pu vacciner la première personne de notre essai de phase III.
L’accélération du lancement des essais cliniques et de la réception des données pourrait changer la donne pour l’approbation des médicaments d’urgence et non urgents à l’avenir, même au-delà des vaccins. Beaucoup de nos médicaments et de nos traitements sont vitaux, et ces traitements sont également nécessaires le plus rapidement possible.
En tant qu’équipe, nous sommes désormais conditionnés pour être résilients face à la nécessité de résoudre des problèmes, de rassembler des gens et de faire preuve de détermination. Tous ces outils sont reproductibles et nous aident à avancer beaucoup plus vite qu’auparavant dans tous nos programmes et toutes nos phases de développement.
McKinsey : Alors que les efforts de vaccination s’étendent à travers le monde, que peut-on faire pour sensibiliser davantage aux vaccins et réduire l’hésitation à se faire vacciner ?
Angela Hwang : Il y a encore beaucoup à faire pour aider le monde et le public à comprendre le compromis risque-bénéfice de ce qui se passe quand on ne se fait pas vacciner. Cette tâche incombe à tous les fabricants de vaccins, ainsi qu’aux gouvernements.
Nous sommes à un bon moment pour intensifier les efforts d’éducation et aider les gens à comprendre pourquoi les vaccinations sont importantes et ce qu’elles signifient réellement pour eux, non seulement en tant qu’individus mais aussi en tant que bienfait pour la santé publique. Lorsque vous vous faites vacciner, il ne s’agit pas seulement de vous empêcher de contracter la maladie. Il s’agit également d’aider à ralentir la transmission du virus, de sorte que la transmission continue et les épidémies dans votre communauté puissent diminuer au fil du temps.
Les données du monde réel en témoignent. Lorsque nous avons réalisé l’essai clinique de notre vaccin COVID-19, plus de 44 000 personnes ont participé à notre étude, et la moitié d’entre elles ont été vaccinées. Aujourd’hui, près d’un quart de la population mondiale a été entièrement vacciné.5 L’analyse rétrospective que nous recueillons dans certains pays est également révélatrice. Israël a publié ses données. Le Royaume-Uni a publié ses données. Les centres américains de contrôle et de prévention des maladies ont publié leurs données. Ces informations seront essentielles pour renforcer la confiance dans les vaccins. Un échantillon de cette taille est incroyablement puissant lorsque vous pouvez l’utiliser pour décrire les expériences vécues par les gens et aider ceux qui hésitent. L’expérience du monde réel ne peut être sous-estimée et contribuera à éduquer les gens afin qu’ils puissent prendre des décisions éclairées sur la vaccination.
À propos de cet article
Ce contenu est fourni « tel quel » uniquement à des fins d’information. Il ne s’agit pas de conseils juridiques, de santé ou de sécurité. Les organisations doivent faire appel à leurs propres experts pour s’assurer que les mesures adoptées sont conformes aux lois et normes en vigueur dans leurs juridictions. Les opinions exprimées par les personnes ou les organisations sont les leurs et ne reflètent pas les vues ou les opinions de McKinsey. Les références à des produits ou organisations spécifiques ne constituent pas une approbation ou une recommandation de McKinsey.
COMIRNATY® (vaccin COVID-19, ARNm)* est un vaccin COVID-19 approuvé par la FDA, fabriqué par Pfizer pour BioNTech. Il est approuvé en tant que série de deux doses pour la prévention du COVID-19 chez les personnes âgées de 16 ans et plus. Il est également autorisé par l’EUA à être administré en cas d’urgence pour prévenir le COVID-19 chez les personnes âgées de 12 à 15 ans et à être fourni en tant que troisième dose aux personnes âgées de 12 ans et plus qui ont été déterminées comme ayant certains types d’immunodépression. Le vaccin Pfizer-BioNTech COVID-19 a reçu une autorisation de mise sur le marché de la FDA pour la prévention du COVID-19 chez les personnes âgées de 12 ans et plus, et pour l’administration d’une troisième dose aux personnes âgées de 12 ans et plus qui présentent certaines déficiences immunitaires. L’utilisation d’urgence du produit n’a pas été approuvée ou homologuée par la FDA mais a été autorisée par la FDA dans le cadre d’un EUA pour prévenir le COVID-19 chez les personnes âgées de 12 ans et plus, et l’utilisation d’urgence de ce produit n’est autorisée que pour la durée de la déclaration selon laquelle il existe des circonstances justifiant l’autorisation de l’utilisation d’urgence du produit médical en vertu de la section 564(b)(1) du FD&C Act, à moins que la déclaration ne soit résiliée ou l’autorisation révoquée plus tôt. Veuillez consulter les informations de prescription complètes (16 ans et plus) et la fiche d’information pour le bénéficiaire et le soignant (12 ans et plus) sur labeling.pfizer.com.
*Le vaccin homologué COMIRNATY® a la même formulation que le vaccin autorisé Pfizer-BioNTech COVID-19, et les produits peuvent être utilisés de manière interchangeable pour assurer la série de vaccinations sans présenter de problèmes de sécurité ou d’efficacité. Les produits sont juridiquement distincts, avec certaines différences qui n’affectent pas la sécurité ou l’efficacité.
Angela Hwang est présidente de groupe de Pfizer Biopharmaceuticals et cadre chez Pfizer. David Quigley est associé principal du bureau new-yorkais de McKinsey.
Cet article a été révisé par Astrid Sandoval, rédactrice exécutive au bureau de Londres.
20 septembre 2021
Titre de ‘article original en anglais : Pfizer’s mix of science and grit alters the course of its COVID-19 response
Traduction : Lelibrepenseur.org avec DeepL Translator






































