Il ne suffit pas de traiter ses adversaires de complotistes ou d’antivax… pour avoir raison, la réalité finira toujours par s’imposer, c’est ainsi que fonctionne le monde depuis toujours.
1. Introduction
La maladie à coronavirus 2019 (COVID-19) causée par le coronavirus 2 du syndrome respiratoire aigu sévère (SRAS-CoV-2) a été annoncée par l’Organisation mondiale de la santé (OMS) comme une pandémie mondiale le 11 mars 2020, et elle est apparue comme une crise sanitaire dévastatrice. En février 2022, le COVID-19 a entraîné plus de 430 millions de cas d’infection signalés et 5,9 millions de décès dans le monde entier [1]. Des vaccins efficaces et sûrs sont nécessaires de toute urgence pour réduire les taux de morbidité et de mortalité associés au COVID-19.
Plusieurs vaccins contre le COVID-19 ont été développés, en particulier des vaccins à ARNm (par Pfizer-BioNTech et Moderna), des vaccins à vecteur adénoviral recombinant défectueux pour la réplication (par Janssen-Johnson and Johnson, Astra-Zeneca, Sputnik-V et CanSino) et des vaccins inactivés (par Sinopharm, Bharat Biotech et Sinovac). Le vaccin à ARNm a l’avantage d’être flexible et efficace dans la conception et la fabrication de l’immunogène, et actuellement, de nombreux candidats vaccins sont à différents stades de développement et d’application. Plus précisément, le vaccin ARNm COVID-19 BNT162b2 développé par Pfizer et BioNTech a été évalué avec succès lors d’essais cliniques [2,3,4] et administré lors de campagnes nationales de vaccination contre le COVID-19 dans différentes régions du monde [5,6,7,8].
BNT162b2 est un vaccin à ARN modifié par des nucléosides (modRNA) encapsulé dans des nanoparticules lipidiques (LNP). Il code pour la totalité de la protéine de pointe (S) du SRAS-CoV-2, modifiée par deux mutations de proline pour assurer une conformation pré-fusionnelle optimale sur le plan antigénique, qui imite le virus intact pour susciter des anticorps neutralisant le virus [3]. Conformément aux essais cliniques randomisés, BNT162b2 a montré une efficacité élevée sur un large éventail de résultats liés au COVID-19 dans un contexte réel [5]. Néanmoins, de nombreux défis restent à relever, notamment la surveillance de la sécurité et de l’efficacité à long terme du vaccin. Cela justifie une évaluation et des investigations supplémentaires. Le profil de sécurité du BNT162b2 n’est actuellement disponible qu’à partir d’études cliniques à court terme. Des effets indésirables moins courants du BNT162b2 ont été signalés, notamment péricardite, arythmie, thrombose veineuse profonde, embolie pulmonaire, infarctus du myocarde, hémorragie intracrânienne et thrombocytopénie [4,9,10,11,12,13,14,15,16,17,18,19,20]. Certaines études font également état d’effets indésirables observés avec d’autres types de vaccins [21,22,23,24]. Pour mieux comprendre les mécanismes qui sous-tendent les effets indésirables liés aux vaccins, des enquêtes cliniques ainsi que des analyses cellulaires et moléculaires sont nécessaires.
Une étude récente a montré que les ARN du SRAS-CoV-2 peuvent faire l’objet d’une transcription inverse et s’intégrer dans le génome des cellules humaines [25]. On peut donc se demander si cela peut également se produire avec BNT162b2, qui code pour un ARN partiel du SRAS-CoV-2. Dans les données pharmacocinétiques fournies par Pfizer à l’Agence européenne des médicaments (EMA), la biodistribution de BNT162b2 a été étudiée chez des souris et des rats par injection intramusculaire de LNP radiomarqué et de modRNA luciférase. La radioactivité a été détectée dans la plupart des tissus dès le premier point temporel (0,25 h), et les résultats ont montré que le site d’injection et le foie étaient les principaux sites de distribution, avec des concentrations maximales observées 8 à 48 h après la dose [26]. En outre, chez les animaux ayant reçu l’injection de BNT162b2, des effets hépatiques réversibles ont été observés, notamment une hypertrophie du foie, une vacuolisation, une augmentation des taux de gamma glutamyl transférase (γGT) et une augmentation des taux d’aspartate transaminase (AST) et d’alcaline phosphatase (ALP) [26]. Des effets hépatiques transitoires induits par les systèmes d’administration de LNP ont été rapportés précédemment [27,28,29,30], néanmoins, il a également été démontré que le LNP vide sans modRNA seul n’introduit aucune lésion hépatique significative [27]. Par conséquent, dans cette étude, nous voulons examiner l’effet de BNT162b2 sur une lignée de cellules hépatiques humaines in vitro et déterminer si BNT162b2 peut être transcrit en ADN par des mécanismes endogènes.2. Matériaux et méthodes
2.1. Culture cellulaire
Les cellules Huh7 (Banque cellulaire JCRB, Osaka, Japon) ont été cultivées à 37 °C, à 5 % de CO2, dans un milieu DMEM (HyClone, HYCLSH30243.01) complété par 10 % (v/v) de sérum bovin fœtal (Sigma-Aldrich, F7524-500ML, Burlington, MA, États-Unis) et 1 % (v/v) de pénicilline-streptomycine (HyClone, SV30010, Logan, UT, États-Unis). Pour le traitement par BNT162b2, les cellules Huh7 ont été ensemencées à une densité de 200 000 cellules/puits dans des plaques à 24 puits. Le vaccin ARNm BNT162b2 (Pfizer BioNTech, New York, NY, États-Unis) a été dilué avec une injection stérile de chlorure de sodium à 0,9 %, USP, jusqu’à une concentration finale de 100 μg/mL, comme décrit dans la directive du fabricant [31]. La suspension de BNT162b2 a ensuite été ajoutée dans les milieux de culture cellulaire pour atteindre des concentrations finales de 0,5, 1,0 ou 2,0 μg/mL. Les cellules Huh7 ont été incubées avec ou sans BNT162b2 pendant 6, 24 et 48 h. Les cellules ont été soigneusement lavées avec du PBS et récoltées par trypsinisation et stockées à -80 °C jusqu’à leur utilisation ultérieure.
2.2. RT-QPCR EN TEMPS RÉEL
L’ARN des cellules a été extrait avec le RNeasy Plus Mini Kit (Qiagen, 74134, Hilden, Allemagne) en suivant le protocole du fabricant. La RT-PCR a été réalisée à l’aide du kit de synthèse d’ADNc de premier brin RevertAid (Thermo Fisher Scientific, K1622, Waltham, MA, USA) en suivant le protocole du fabricant. La qPCR en temps réel a été réalisée en utilisant le mélange maître Maxima SYBR Green/ROX qPCR (Thermo Fisher Scientific, K0222, Waltham, MA, USA) avec des amorces pour BNT162b2, LINE-1 et les gènes domestiques ACTB et GAPDH (Tableau 1).
Tableau 1. Séquences d’amorces de la RT-qPCR et de la PCR.
2.3. Coloration par immunofluorescence et imagerie confocale
Les cellules Huh7 ont été cultivées dans des lames à huit chambres (LAB-TEK, 154534, Santa Cruz, CA, USA) avec une densité de 40 000 cellules/puits, avec ou sans BNT162b2 (0,5, 1 ou 2 µg/mL) pendant 6 heures. L’immunohistochimie a été réalisée en utilisant l’anticorps primaire anti-LINE-1 ORF1p monoclonal de souris (Merck, 3574308, Kenilworth, NJ, USA), l’anticorps secondaire Cy3 Donkey anti-mouse (Jackson ImmunoResearch, West Grove, PA, USA), et le Hoechst (Life technologies, 34850, Carlsbad, CA, USA), selon le protocole de Thermo Fisher (Waltham, MA, USA). Deux images par condition ont été prises à l’aide d’un Zeiss LSM 800 et d’un objectif à immersion d’huile 63X, et l’intensité de la coloration a été quantifiée sur la zone individuelle de la cellule entière et la zone du noyau sur 15 cellules par image par ImageJ 1.53c. L’intensité de la coloration LINE-1 pour le cytosol a été calculée en soustrayant l’intensité du noyau de celle de la cellule entière. Un numéro aléatoire a été attribué à toutes les images des cellules afin d’éviter tout biais. Pour marquer les noyaux (déterminés par la coloration Hoechst) et les cellules entières (déterminées par les limites de la fluorescence LINE-1), l’outil de sélection à main levée a été utilisé. Ces zones ont ensuite été mesurées, et l’intensité moyenne a été utilisée pour comparer les groupes.
2.4. Purification de l’ADN génomique, amplification par PCR, purification sur gel d’agarose et séquençage Sanger
L’ADN génomique a été extrait des culots cellulaires avec le tampon PBND (10 mM Tris-HCl pH 8,3, 50 mM KCl, 2,5 mM MgCl2, 0,45 % NP-40, 0,45 % Tween-20) selon le protocole décrit précédemment [32]. Pour éliminer l’ARN résiduel de la préparation d’ADN, de la RNase (100 µg/mL, Qiagen, Hilden, Allemagne) a été ajoutée à la préparation d’ADN et incubée à 37 °C pendant 3 h, suivie de 5 min à 95 °C. La PCR a ensuite été réalisée à l’aide d’amorces ciblant BNT162b2 (les séquences sont indiquées dans le tableau 1), avec le programme suivant : 5 min à 95 °C, 35 cycles de 95 °C pendant 30 s, 58 °C pendant 30 s, et 72 °C pendant 1 min ; enfin, 72 °C pendant 5 min et 12 °C pendant 5 min. Les produits PCR ont été analysés sur un gel d’agarose à 1,4 % (p/v). Les bandes correspondant aux amplicons de la taille attendue (444 bps) ont été découpées et l’ADN a été extrait à l’aide du kit de purification QIAquick PCR (Qiagen, 28104, Hilden, Allemagne), selon les instructions du fabricant. La séquence de l’amplicon d’ADN a été vérifiée par séquençage Sanger (Eurofins Genomics, Ebersberg, Allemagne).
Statistiques
Les comparaisons statistiques ont été effectuées à l’aide du test t de Student bilatéral et de l’ANOVA. Les données sont exprimées en tant que moyenne ± SEM ou ± SD. Les différences avec p < 0,05 sont considérées comme significatives.
2.5. Déclarations éthiques
La lignée cellulaire Huh7 a été obtenue auprès de la banque cellulaire de la Japanese Collection of Research Bioresources (JCRB).3. Résultats
3.1. BNT162b2 pénètre dans les cellules de la lignée cellulaire hépatique humaine Huh7 avec une grande efficacité
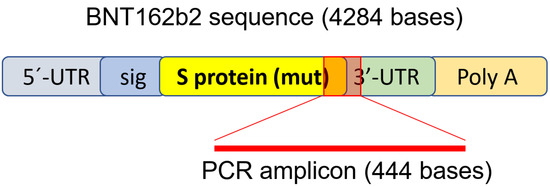
Pour déterminer si le BNT162b2 pénètre dans les cellules hépatiques humaines, nous avons exposé la lignée cellulaire hépatique humaine Huh7 au BNT162b2. Dans une étude précédente sur la cinétique d’absorption des LNP dans les cellules Huh7, l’efficacité biologique maximale des LNP a été observée entre 4 et 7 heures [33]. Par conséquent, dans notre étude, les cellules Huh7 ont été cultivées avec ou sans concentrations croissantes de BNT162b2 (0,5, 1,0 et 2,0 µg/mL) pendant 6, 24 et 48 h. L’ARN a été extrait des cellules et une réaction en chaîne par polymérase de transcription inverse quantitative en temps réel (RT-qPCR) a été réalisée en utilisant des amorces ciblant la séquence de BNT162b2, comme illustré dans la Figure 1. La séquence complète de BNT162b2 est disponible publiquement [34] et contient une coiffe de deux nucléotides ; la région 5′- non traduite (UTR) qui incorpore la 5′ -UTR d’un gène α-globine humain ; la longueur totale de la protéine S du SRAS-CoV-2 avec deux mutations de proline ; la région 3′-UTR qui incorpore le segment de l’ARNr 12S mitochondrial humain (mtRNR1) et le segment du gène AES/TLE5 humain avec deux mutations C→U ; la queue poly(A). L’analyse détaillée de la séquence de la protéine S dans BNT162b2 a révélé 124 séquences identiques à 100 % aux séquences génomiques humaines et trois séquences présentant une seule discordance de nucléotides (nt) dans 19-26 nts (tableau S1, voir Matériaux supplémentaires). Pour détecter le niveau d’ARN de BNT162b2, nous avons conçu des amorces dont l’amorce directe est située dans les régions de la protéine S du SRAS-CoV-2 et l’amorce inverse dans le 3′-UTR, ce qui permet la détection de l’amplicon PCR unique de BNT162b2 sans liaison non spécifique des amorces aux régions génomiques humaines.
Figure 1. Jeu d’amorces PCR utilisé pour détecter le niveau d’ARNm et la transcription inverse de BNT162b2. L’illustration de BNT162b2 a été adaptée de la littérature décrite précédemment [34].
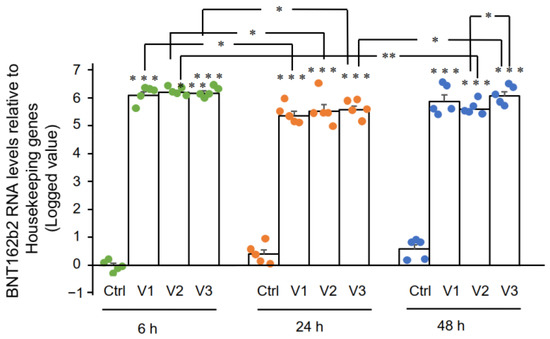
Les résultats de la RT-qPCR ont montré que les cellules Huh7 traitées avec BNT162b2 présentaient des niveaux élevés d’ARNm BNT162b2 par rapport aux gènes domestiques à 6, 24 et 48 h (figure 2, présentée en log 2-ΔΔCT en raison des niveaux exceptionnellement élevés). Les trois concentrations de BNT162b2 ont conduit à des niveaux intracellulaires d’ARNm de BNT162b2 similaires aux différents points dans le temps, sauf que la différence significative entre 1,0 et 2,0 µg/mL a été observée à 48 h. Les niveaux d’ARNm de BNT162b2 ont diminué de manière significative à 24 h par rapport à 6 h, mais ont augmenté à nouveau à 48 h.
Figure 2. Niveaux d’ARNm de BNT162b2 dans les cellules Huh7 traitées avec BNT162b2.Les cellules Huh7 ont été traitées sans (Ctrl) ou avec 0,5 (V1), 1 (V2) et 2 µg/mL (V3) de BNT162b2 pendant 6 (points verts), 24 (points orange) et 48 h (points bleus). L’ARN a été purifié et la qPCR a été réalisée en utilisant des amorces ciblant BNT162b2. Les niveaux d’ARN de BNT162b2 sont présentés sous forme de valeurs logarithmiques 2-ΔΔCT par rapport aux gènes domestiques GAPDH et ACTB. Les résultats proviennent de cinq expériences indépendantes (n = 5). Les différences entre les groupes respectifs ont été analysées à l’aide du test t de Student bilatéral. Les données sont exprimées en tant que moyenne ± SEM. (* p < 0,05 ; ** p < 0,01 ; *** p < 0,001 par rapport au contrôle respectif à chaque point temporel, ou comme indiqué).
3.2. Effet de BNT162b2 sur la transcriptase inverse endogène humaine Long Interspersed Nuclear Element-1 (LINE-1)
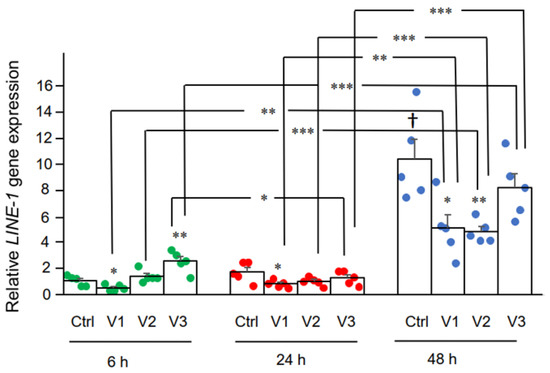
Nous avons examiné ici l’effet de BNT162b2 sur l’expression du gène LINE-1. Une RT-qPCR a été réalisée sur de l’ARN purifié à partir de cellules Huh7 traitées par BNT162b2 (0, 0,5, 1,0 et 2,0 µg/mL) pendant 6, 24 et 48 heures, en utilisant des amorces ciblant LINE-1. Une augmentation significative de l’expression de LINE-1 par rapport au contrôle a été observée à 6 h avec 2,0 µg/mL de BNT162b2, tandis que des concentrations plus faibles de BNT162b2 ont diminué l’expression de LINE-1 à tous les points temporels (Figure 3).
Figure 3. Niveaux d’ARNm de LINE-1 dans les cellules Huh7 traitées avec BNT162b2.Les cellules Huh7 ont été traitées sans (Ctrl) ou avec 0,5 (V1), 1 (V2), et 2 µg/mL (V3) de BNT162b2 pendant 6 (points verts), 24 (points rouges), et 48 h (points bleus). L’ARN a été purifié et la qPCR a été réalisée en utilisant des amorces ciblant LINE-1. Les niveaux d’ARN de LINE-1 sont présentés sous forme de valeurs 2-ΔΔCT par rapport aux gènes de référence GAPDH et ACTB. Les résultats proviennent de cinq expériences indépendantes (n = 5). Les différences entre les groupes respectifs ont été analysées à l’aide du test t de Student bilatéral. Les données sont exprimées en tant que moyenne ± SEM. (* p < 0,05 ; ** p < 0,01 ; *** p < 0,001 par rapport au contrôle respectif à chaque point temporel, ou comme indiqué ; † p < 0,05 par rapport à 6 h-Ctrl).
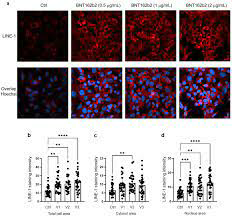
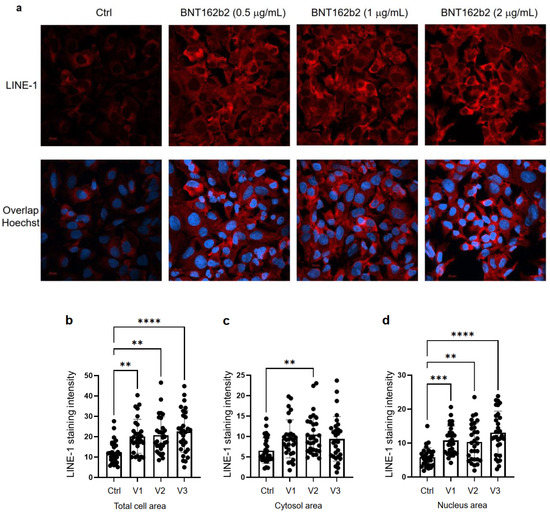
Ensuite, nous avons étudié l’effet de BNT162b2 sur le niveau de la protéine LINE-1. Le LINE-1 complet est constitué d’une région 5′ non traduite (UTR), de deux cadres de lecture ouverts (ORF), ORF1 et ORF2, et d’un 3′UTR, dont l’ORF1 est une protéine de liaison à l’ARN ayant une activité chaperonne. Il a été démontré que l’activité de rétrotransposition de LINE-1 implique la translocation de l’ORF1 dans le noyau [35]. Les cellules Huh7 traitées avec ou sans BNT162b2 (0,5, 1,0 et 2,0 µg/mL) pendant 6 h ont été fixées et colorées avec des anticorps se liant à l’ORF1p de LINE-1, et la sonde Hoechst spécifique de l’ADN pour la visualisation du noyau cellulaire (Figure 4a). La quantification de l’intensité de la coloration par immunofluorescence a montré que le BNT162b2 augmentait les niveaux de protéine LINE-1 ORF1p à la fois dans la zone de la cellule entière et dans le noyau à toutes les concentrations testées (Figure 4b-d).
Figure 4. Immunohistochimie de cellules Huh7 traitées avec BNT162b2 sur la distribution de la protéine LINE-1.Les cellules Huh7 ont été traitées sans (Ctrl) ou avec 0,5, 1 et 2 µg/mL de BNT162b2 pendant 6 h. Les cellules ont été fixées et colorées avec des anticorps se liant à l’ORF1p de LINE-1 (rouge) et la sonde Hoechst spécifique de l’ADN pour la visualisation du noyau cellulaire (bleu). (a) Images représentatives de l’expression de LINE-1 dans les cellules Huh7 traitées avec ou sans BNT162b2. (b-d) Quantification de la protéine LINE-1 dans la zone de la cellule entière (b), le cytosol (c) et le noyau (d). Toutes les données ont été analysées à l’aide d’une ANOVA à une voie, et les graphiques ont été créés à l’aide de GraphPad Prism V 9.2. Toutes les données sont présentées en tant que moyenne ± SD (** p < 0,01 ; *** p < 0,001 ; **** p < 0,0001 comme indiqué).
3.3. Détection de l’ADN de BNT162b2 transcrit en sens inverse dans les cellules Huh7
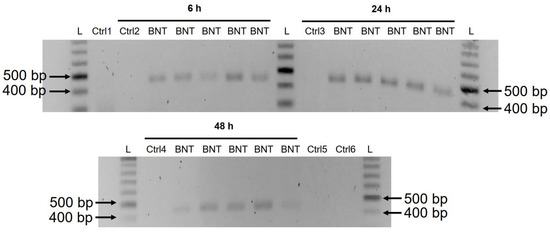
Une étude précédente a montré que l’entrée de la protéine LINE-1 dans le noyau est associée à la rétrotransposition [35]. Dans l’expérience de coloration par immunofluorescence décrite ci-dessus, des niveaux accrus de LINE-1 dans le noyau ont été observés dès la plus faible concentration de BNT162b2 (0,5 µg/mL). Pour examiner si le BNT162b2 est transcrit de manière inverse dans l’ADN lorsque le niveau de LINE-1 est élevé, nous avons purifié l’ADN génomique des cellules Huh7 traitées avec 0,5 µg/mL de BNT162b2 pendant 6, 24 et 48 h. L’ADN purifié a été traité avec de la RNase pour éliminer l’ARN et soumis à la PCR en utilisant des amorces ciblant le BNT162b2, comme illustré dans la Figure 1. Les fragments d’ADN amplifiés ont ensuite été visualisés par électrophorèse et purifiés sur gel (Figure 5). Des amplicons d’ADN BNT162b2 ont été détectés aux trois points de temps (6, 24 et 48 h). Le séquençage Sanger a confirmé que les amplicons d’ADN étaient identiques à la séquence BNT162b2 flanquée par les amorces (tableau 2). Pour s’assurer que les amplicons d’ADN provenaient bien de l’ADN et non de l’ARN de BNT162b2, nous avons également effectué une PCR sur l’ARN purifié à partir de cellules Huh7 traitées avec 0,5 µg/mL de BNT162b2 pendant 6 h, avec ou sans traitement à la RNase (Ctrl 5 et 6 dans la Figure 5), et aucun amplicon n’a été détecté dans les échantillons d’ARN soumis à la PCR.
Figure 5. Détection des amplicons d’ADN de BNT162b2 dans les cellules Huh7 traitées avec BNT162b2.Les cellules Huh7 ont été traitées sans (Ctrl) ou avec 0,5 µg/mL de BNT162b2 pendant 6, 24 et 48 h. L’ADN génomique a été purifié et digéré avec 100 µg/mL de RNase. La PCR a été effectuée sur tous les échantillons avec des amorces ciblant BNT162b2, comme indiqué dans la figure 1 et le tableau 1. Les amplicons d’ADN (444 bps) ont été visualisés sur gel d’agarose. BNT : BNT162b2 ; L : échelle d’ADN ; Ctrl1 : cellules Huh7 cultivées ; Ctrl2 : Cellules Huh7 sans traitement BNT162b2, prélevées à 6 h ; Ctrl3 : Cellules Huh7 sans traitement BNT162b2 prélevées à 24 h ; Ctrl4 : Cellules Huh7 sans traitement BNT162b2 prélevées à 48 h ; Ctrl5 : ARN de cellules Huh7 traitées avec 0,5 µg/mL de BNT162b2 pendant 6 h ; Ctrl6 : ARN de cellules Huh7 traitées avec 0,5 µg/mL de BNT162b2 pendant 6 h, digéré avec de la RNase.
Tableau 2. Résultat du séquençage Sanger de l’amplicon
BNT162b2.
4. Discussion
Dans cette étude, nous présentons des preuves que l’ARNm BNT162b2 du vaccin COVID-19 est capable de pénétrer dans la lignée cellulaire du foie humain Huh7 in vitro. L’ARNm BNT162b2 est transcrit de manière inverse dans les cellules en ADN aussi rapidement que 6 heures après l’exposition au BNT162b2. Un mécanisme possible de transcription inverse est la transcriptase inverse endogène LINE-1, et la distribution de la protéine LINE-1 dans le noyau est élevée par le BNT162b2.
L’accumulation intracellulaire de la LNP dans les hépatocytes a été démontrée in vivo [36]. Une étude préclinique sur BNT162b2 a montré que BNT162b2 pénètre dans la lignée cellulaire humaine HEK293T et conduit à une expression robuste de l’antigène BNT162b2 [37]. Par conséquent, dans cette étude, nous avons d’abord examiné l’entrée de BNT162b2 dans la lignée de cellules hépatiques humaines Huh7. Le choix des concentrations de BNT162b2 utilisées dans cette étude mérite une explication. BNT162b2 est administré en une série de deux doses à trois semaines d’intervalle, et chaque dose contient 30 µg de BNT162b2 dans un volume de 0,3 ml, ce qui fait que la concentration locale au site d’injection est au maximum de 100 µg/ml [31]. Une étude précédente sur des vaccins à ARNm contre les virus de la grippe H10N8 et H7N9 utilisant un système d’administration LNP similaire a montré que le vaccin à ARNm peut se distribuer de manière plutôt non spécifique dans plusieurs organes tels que le foie, la rate, le cœur, les reins, les poumons et le cerveau, et que la concentration dans le foie est environ 100 fois inférieure à celle du site d’injection intramusculaire [38]. Dans le rapport d’évaluation du BNT162b2 fourni à l’EMA par Pfizer, les études de distribution pharmacocinétique chez le rat ont démontré qu’une proportion relativement importante (jusqu’à 18%) de la dose totale se distribue dans le foie [26]. Nous avons donc choisi d’utiliser 0,5, 1 et 2 μg/mL de vaccin dans nos expériences sur les cellules hépatiques. Cependant, l’effet d’une gamme plus large de concentrations inférieures et supérieures de BNT162b2 devrait également être vérifié dans des études futures.
Dans l’étude actuelle, nous avons utilisé une lignée de cellules hépatiques humaines pour l’étude in vitro. Il est intéressant d’examiner si les cellules hépatiques présentent également la protéine de pointe du SRAS-CoV-2 dérivée du vaccin, ce qui pourrait potentiellement faire des cellules hépatiques des cibles pour les cellules T cytotoxiques réactives à la protéine de pointe préalablement amorcées. On a signalé des cas de personnes ayant développé une hépatite auto-immune [39] après une vaccination par BNT162b2. Pour mieux comprendre les effets potentiels de BNT162b2 sur la fonction hépatique, des modèles in vivo sont nécessaires pour les études futures.
Dans le rapport de toxicité de BNT162b2, aucune étude de génotoxicité ou de cancérogénicité n’a été fournie [26]. Notre étude montre que le BNT162b2 peut être transcrit de façon inverse en ADN dans la lignée de cellules hépatiques Huh7, ce qui peut soulever la question de savoir si l’ADN dérivé du BNT162b2 peut être intégré dans le génome de l’hôte et affecter l’intégrité de l’ADN génomique, ce qui peut potentiellement provoquer des effets secondaires génotoxiques. À ce stade, nous ne savons pas si l’ADN transcrit en sens inverse à partir de BNT162b2 est intégré dans le génome cellulaire. D’autres études sont nécessaires pour démontrer l’effet de BNT162b2 sur l’intégrité génomique, notamment le séquençage du génome entier des cellules exposées à BNT162b2, ainsi que des tissus de sujets humains ayant reçu la vaccination par BNT162b2.
Le rétrotransposon autonome humain LINE-1 est une transcriptase inverse endogène cellulaire et le seul transposon actif restant chez l’homme, capable de se rétrotransposer et de rétrotransposer d’autres éléments non autonomes [40,41], et ~17% du génome humain sont constitués de séquences LINE-1 [42]. Les éléments Alu non autonomes, les éléments nucléotidiques courts et dispersés (SINE), les répétitions en tandem à nombre variable (VNTR), ainsi que les pseudogènes traités par l’ARNm cellulaire, sont rétrotransposés par les protéines de rétrotransposition LINE-1 travaillant en trans [43,44]. Une étude récente a montré que la protéine LINE-1 endogène sert de médiateur à la transcription inverse et à l’intégration des séquences du SRAS-CoV-2 dans les génomes des cellules humaines infectées [25]. De plus, l’expression de LINE-1 endogène est souvent augmentée lors d’une infection virale, y compris l’infection par le SRAS-CoV-2 [45,46,47]. Des études antérieures ont montré que l’activité de rétrotransposition de LINE-1 est régulée par le métabolisme de l’ARN [48,49], la réponse aux lésions de l’ADN [50] et l’autophagie [51]. La rétrotransposition efficace de LINE-1 est souvent associée au cycle cellulaire et à la rupture de l’enveloppe nucléaire pendant la mitose [52,53], ainsi qu’aux rétrovirus exogènes [54,55], ce qui favorise l’entrée de LINE-1 dans le noyau. Dans notre étude, nous avons observé une augmentation de la distribution de l’ORF1p de LINE-1 déterminée par immunohistochimie dans le noyau par BNT162b2 à toutes les concentrations testées (0,5, 1 et 2 μg/mL), tandis qu’une expression génétique élevée de LINE-1 a été détectée à la plus forte concentration de BNT162b2 (2 μg/mL). Il convient de noter que la transcription des gènes est régulée par les modifications de la chromatine, la régulation des facteurs de transcription et le taux de dégradation de l’ARN, tandis que la régulation traductionnelle des protéines implique le recrutement des ribosomes sur le codon d’initiation, la modulation de l’élongation des peptides, la fin de la synthèse des protéines ou la biogenèse des ribosomes.Ces deux processus sont contrôlés par des mécanismes différents, et il se peut donc qu’ils ne présentent pas toujours les mêmes schémas de changement en réponse à des défis externes. La régulation exacte de l’activité de LINE-1 en réponse à BNT162b2 mérite une étude plus approfondie.Le modèle cellulaire que nous avons utilisé dans cette étude est une lignée cellulaire de carcinome, avec une réplication active de l’ADN qui diffère des cellules somatiques non-divisées. Il a également été démontré que les cellules Huh7 présentent des différences significatives dans l’expression des gènes et des protéines, notamment la régulation des protéines impliquées dans le métabolisme de l’ARN [56]. Cependant, la prolifération cellulaire est également active dans plusieurs tissus humains tels que la moelle osseuse ou les couches basales des épithéliums, ainsi que pendant l’embryogenèse, et il est donc nécessaire d’examiner l’effet de BNT162b2 sur l’intégrité génomique dans ces conditions. En outre, une rétrotransposition efficace de LINE-1 a également été signalée dans des cellules non divisées et terminalement différenciées, telles que les neurones humains [57,58].
Le rapport d’évaluation de Pfizer EMA a également montré que le BNT162b2 se distribue dans la rate (<1,1%), les glandes surrénales (<0,1%), ainsi qu’une radioactivité faible et mesurable dans les ovaires et les testicules (<0,1%) [26]. De plus, aucune donnée sur le transfert placentaire du BNT162b2 n’est disponible dans le rapport d’évaluation de Pfizer EMA. Nos résultats ont montré que l’ARNm du BNT162b2 pénètre facilement dans les cellules Huh7 à une concentration (0,5 µg/mL) correspondant à 0,5 % de la concentration locale du site d’injection, induit des changements dans l’expression du gène et de la protéine LINE-1, et dans les 6 heures, la transcription inverse du BNT162b2 peut être détectée. Il est donc important d’étudier plus avant l’effet de BNT162b2 sur d’autres types de cellules et de tissus, in vitro et in vivo.5. Conclusions
Notre étude est la première étude in vitro sur l’effet de l’ARNm BNT162b2 du vaccin COVID-19 sur une lignée de cellules hépatiques humaines. Nous présentons des preuves de l’entrée rapide de BNT162b2 dans les cellules et de la transcription inverse intracellulaire ultérieure de l’ARNm BNT162b2 en ADN.
Matériel supplémentaire
Les informations complémentaires suivantes peuvent être téléchargées à l’adresse suivante : https://www.mdpi.com/article/10.3390/cimb44030073/s1.
Contributions des auteurs
M.A., F.O.F., D.Y., M.B. et C.L. ont réalisé les expériences in vitro. M.A. et F.O.F. ont effectué l’analyse des données. M.R. et Y.D.M. ont contribué à la mise en œuvre de la recherche, ont conçu et supervisé l’étude. Y.D.M. a rédigé l’article avec la contribution de tous les auteurs. Tous les auteurs ont lu et approuvé la version publiée du manuscrit.Financement
Cette étude a été soutenue par le Conseil suédois de la recherche, Strategic Research Area Exodiab, Dnr 2009-1039, le Fonds du gouvernement suédois pour la recherche clinique (ALF) et la fondation de l’hôpital universitaire de Scanie.Déclaration du conseil d’examen institutionnel
Non applicable.
Déclaration de consentement éclairé
Sans objet.Déclaration de disponibilité des données
Toutes les données étayant les résultats de cette étude sont disponibles dans l’article et les informations complémentaires.
Remerciements
Les auteurs remercient Sven Haidl, Maria Josephson, Enming Zhang, Jia-Yi Li, Caroline Haikal et Pradeep Bompada pour leur soutien à cette étude.Conflits d’intérêts
Les auteurs ne déclarent aucun conflit d’intérêt.Références
World Health Organization. Coronavirus (COVID-19) Dashboard. Available online: https://covid19.who.int/ (accessed on 22 February 2022).
Mulligan, M.J.; Lyke, K.E.; Kitchin, N.; Absalon, J.; Gurtman, A.; Lockhart, S.; Neuzil, K.; Raabe, V.; Bailey, R.; Swanson, K.A.; et al. Phase I/II study of COVID-19 RNA vaccine BNT162b1 in adults. Nature 2020, 586, 589–593. [Google Scholar] [CrossRef] [PubMed]
Walsh, E.E.; Frenck, R.W., Jr.; Falsey, A.R.; Kitchin, N.; Absalon, J.; Gurtman, A.; Lockhart, S.; Neuzil, K.; Mulligan, M.J.; Bailey, R.; et al. Safety and Immunogenicity of Two RNA-Based COVID-19 Vaccine Candidates. N. Engl. J. Med. 2020, 383, 2439–2450. [Google Scholar] [CrossRef] [PubMed]
Polack, F.P.; Thomas, S.J.; Kitchin, N.; Absalon, J.; Gurtman, A.; Lockhart, S.; Perez, J.L.; Perez Marc, G.; Moreira, E.D.; Zerbini, C.; et al. Safety and Efficacy of the BNT162b2 mRNA COVID-19 Vaccine. N. Engl. J. Med. 2020, 383, 2603–2615. [Google Scholar] [CrossRef] [PubMed]
Harris, R.J.; Hall, J.A.; Zaidi, A.; Andrews, N.J.; Dunbar, J.K.; Dabrera, G. Effect of Vaccination on Household Transmission of SARS-CoV-2 in England. N. Engl. J. Med. 2021, 385, 759–760. [Google Scholar] [CrossRef]
Butt, A.A.; Omer, S.B.; Yan, P.; Shaikh, O.S.; Mayr, F.B. SARS-CoV-2 Vaccine Effectiveness in a High-Risk National Population in a Real-World Setting. Ann. Intern. Med. 2021, 174, 1404–1408. [Google Scholar] [CrossRef]
Dagan, N.; Barda, N.; Kepten, E.; Miron, O.; Perchik, S.; Katz, M.A.; Hernan, M.A.; Lipsitch, M.; Reis, B.; Balicer, R.D. BNT162b2 mRNA Covid-19 Vaccine in a Nationwide Mass Vaccination Setting. N. Engl. J. Med. 2021, 384, 1412–1423. [Google Scholar] [CrossRef]
Rossman, H.; Shilo, S.; Meir, T.; Gorfine, M.; Shalit, U.; Segal, E. COVID-19 dynamics after a national immunization program in Israel. Nat. Med. 2021, 27, 1055–1061. [Google Scholar] [CrossRef]
Fan, B.E.; Shen, J.Y.; Lim, X.R.; Tu, T.M.; Chang, C.C.R.; Khin, H.S.W.; Koh, J.S.; Rao, J.P.; Lau, S.L.; Tan, G.B.; et al. Cerebral venous thrombosis post BNT162b2 mRNA SARS-CoV-2 vaccination: A black swan event. Am. J. Hematol. 2021, 96, E357–E361. [Google Scholar] [CrossRef]
Larson, K.F.; Ammirati, E.; Adler, E.D.; Cooper, L.T., Jr.; Hong, K.N.; Saponara, G.; Couri, D.; Cereda, A.; Procopio, A.; Cavalotti, C.; et al. Myocarditis After BNT162b2 and mRNA-1273 Vaccination. Circulation 2021, 144, 506–508. [Google Scholar] [CrossRef]
Menni, C.; Klaser, K.; May, A.; Polidori, L.; Capdevila, J.; Louca, P.; Sudre, C.H.; Nguyen, L.H.; Drew, D.A.; Merino, J.; et al. Vaccine side-effects and SARS-CoV-2 infection after vaccination in users of the COVID Symptom Study app in the UK: A prospective observational study. Lancet Infect. Dis. 2021, 21, 939–949. [Google Scholar] [CrossRef]
Hansen, T.; Titze, U.; Kulamadayil-Heidenreich, N.S.A.; Glombitza, S.; Tebbe, J.J.; Rocken, C.; Schulz, B.; Weise, M.; Wilkens, L. First case of postmortem study in a patient vaccinated against SARS-CoV-2. Int. J. Infect. Dis. 2021, 107, 172–175. [Google Scholar] [CrossRef] [PubMed]
Kadali, R.A.K.; Janagama, R.; Peruru, S.; Malayala, S.V. Side effects of BNT162b2 mRNA COVID-19 vaccine: A randomized, cross-sectional study with detailed self-reported symptoms from healthcare workers. Int. J. Infect. Dis. 2021, 106, 376–381. [Google Scholar] [CrossRef] [PubMed]
Parkash, O.; Sharko, A.; Farooqi, A.; Ying, G.W.; Sura, P. Acute Pancreatitis: A Possible Side Effect of COVID-19 Vaccine. Cureus 2021, 13, e14741. [Google Scholar] [CrossRef] [PubMed]
Mazzatenta, C.; Piccolo, V.; Pace, G.; Romano, I.; Argenziano, G.; Bassi, A. Purpuric lesions on the eyelids developed after BNT162b2 mRNA COVID-19 vaccine: Another piece of SARS-CoV-2 skin puzzle? J. Eur. Acad. Dermatol. Venereol. 2021, 35, e543–e545. [Google Scholar] [CrossRef]
Lee, E.J.; Cines, D.B.; Gernsheimer, T.; Kessler, C.; Michel, M.; Tarantino, M.D.; Semple, J.W.; Arnold, D.M.; Godeau, B.; Lambert, M.P.; et al. Thrombocytopenia following Pfizer and Moderna SARS-CoV-2 vaccination. Am. J. Hematol. 2021, 96, 534–537. [Google Scholar] [CrossRef]
Ishay, Y.; Kenig, A.; Tsemach-Toren, T.; Amer, R.; Rubin, L.; Hershkovitz, Y.; Kharouf, F. Autoimmune phenomena following SARS-CoV-2 vaccination. Int. Immunopharmacol. 2021, 99, 107970. [Google Scholar] [CrossRef]
Das, B.B.; Kohli, U.; Ramachandran, P.; Nguyen, H.H.; Greil, G.; Hussain, T.; Tandon, A.; Kane, C.; Avula, S.; Duru, C.; et al. Myopericarditis following mRNA COVID-19 Vaccination in Adolescents 12 through 18 Years of Age. J. Pediatr. 2021, 238, 26–32.e1. [Google Scholar] [CrossRef]
McLaurin-Jiang, S.; Garner, C.D.; Krutsch, K.; Hale, T.W. Maternal and Child Symptoms Following COVID-19 Vaccination Among Breastfeeding Mothers. Breastfeed. Med. 2021, 16, 702–709. [Google Scholar] [CrossRef]
Barda, N.; Dagan, N.; Ben-Shlomo, Y.; Kepten, E.; Waxman, J.; Ohana, R.; Hernan, M.A.; Lipsitch, M.; Kohane, I.; Netzer, D.; et al. Safety of the BNT162b2 mRNA Covid-19 Vaccine in a Nationwide Setting. N. Engl. J. Med. 2021, 385, 1078–1090. [Google Scholar] [CrossRef]
Baden, L.R.; El Sahly, H.M.; Essink, B.; Kotloff, K.; Frey, S.; Novak, R.; Diemert, D.; Spector, S.A.; Rouphael, N.; Creech, C.B.; et al. Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine. N. Engl. J. Med. 2021, 384, 403–416. [Google Scholar] [CrossRef]
Sadoff, J.; Gray, G.; Vandebosch, A.; Cardenas, V.; Shukarev, G.; Grinsztejn, B.; Goepfert, P.A.; Truyers, C.; Fennema, H.; Spiessens, B.; et al. Safety and Efficacy of Single-Dose Ad26.COV2.S Vaccine against Covid-19. N. Engl. J. Med. 2021, 384, 2187–2201. [Google Scholar] [CrossRef] [PubMed]
Eichinger, S.; Warkentin, T.E.; Greinacher, A. Thrombotic Thrombocytopenia after ChAdOx1 nCoV-19 Vaccination. Reply. N. Engl. J. Med. 2021, 385, e11. [Google Scholar] [CrossRef] [PubMed]
Doroftei, B.; Ciobica, A.; Ilie, O.D.; Maftei, R.; Ilea, C. Mini-Review Discussing the Reliability and Efficiency of COVID-19 Vaccines. Diagnostics 2021, 11, 579. [Google Scholar] [CrossRef]
Zhang, L.; Richards, A.; Barrasa, M.I.; Hughes, S.H.; Young, R.A.; Jaenisch, R. Reverse-transcribed SARS-CoV-2 RNA can integrate into the genome of cultured human cells and can be expressed in patient-derived tissues. Proc. Natl. Acad. Sci. USA 2021, 118, e2105968118. [Google Scholar] [CrossRef] [PubMed]
Available online: https://www.ema.europa.eu/en/documents/assessment-report/comirnaty-epar-public-assessment-report_en.pdf (accessed on 24 February 2022).
Tanaka, H.; Takata, N.; Sakurai, Y.; Yoshida, T.; Inoue, T.; Tamagawa, S.; Nakai, Y.; Tange, K.; Yoshioka, H.; Maeki, M.; et al. Delivery of Oligonucleotides Using a Self-Degradable Lipid-Like Material. Pharmaceutics 2021, 13, 544. [Google Scholar] [CrossRef]
Sedic, M.; Senn, J.J.; Lynn, A.; Laska, M.; Smith, M.; Platz, S.J.; Bolen, J.; Hoge, S.; Bulychev, A.; Jacquinet, E.; et al. Safety Evaluation of Lipid Nanoparticle-Formulated Modified mRNA in the Sprague-Dawley Rat and Cynomolgus Monkey. Vet. Pathol. 2018, 55, 341–354. [Google Scholar] [CrossRef]
Sato, Y.; Matsui, H.; Yamamoto, N.; Sato, R.; Munakata, T.; Kohara, M.; Harashima, H. Highly specific delivery of siRNA to hepatocytes circumvents endothelial cell-mediated lipid nanoparticle-associated toxicity leading to the safe and efficacious decrease in the hepatitis B virus. J. Control. Release 2017, 266, 216–225. [Google Scholar] [CrossRef]
Heidel, J.D.; Yu, Z.; Liu, J.Y.; Rele, S.M.; Liang, Y.; Zeidan, R.K.; Kornbrust, D.J.; Davis, M.E. Administration in non-human primates of escalating intravenous doses of targeted nanoparticles containing ribonucleotide reductase subunit M2 siRNA. Proc. Natl. Acad. Sci. USA 2007, 104, 5715–5721. [Google Scholar] [CrossRef]
Available online: https://www.cvdvaccine-us.com/ (accessed on 24 February 2022).
Available online: http://bridgeslab.sph.umich.edu/protocols/index.php/Preparation_of_Tail_Samples_(for_Genotyping) (accessed on 24 February 2022).
Gallud, A.; Munson, M.J.; Liu, K.; Idstrom, A.; Barriga, H.M.; Tabaei, S.; Aliakbarinodehi, N.; Ojansivu, M.; Lubart, Q.; Doutch, J.J.; et al. Time evolution of PEG-shedding and serum protein coronation determines the cell uptake kinetics and delivery of lipid nanoparticle. bioRxiv 2021. [Google Scholar] [CrossRef]
World Health Organization Messenger RNA Encoding the Full-Length SARS-CoV-2 Spike Glycoprotein. 2020. Available online: https://web.archive.org/web/20210105162941/https://mednet-communities.net/inn/db/media/docs/11889.doc (accessed on 24 February 2022).
Mita, P.; Wudzinska, A.; Sun, X.; Andrade, J.; Nayak, S.; Kahler, D.J.; Badri, S.; LaCava, J.; Ueberheide, B.; Yun, C.Y.; et al. LINE-1 protein localization and functional dynamics during the cell cycle. Elife 2018, 7, e30058. [Google Scholar] [CrossRef]
Sato, Y.; Kinami, Y.; Hashiba, K.; Harashima, H. Different kinetics for the hepatic uptake of lipid nanoparticles between the apolipoprotein E/low density lipoprotein receptor and the N-acetyl-d-galactosamine/asialoglycoprotein receptor pathway. J. Control. Release 2020, 322, 217–226. [Google Scholar] [CrossRef]
Vogel, A.B.; Kanevsky, I.; Che, Y.; Swanson, K.A.; Muik, A.; Vormehr, M.; Kranz, L.M.; Walzer, K.C.; Hein, S.; Guler, A.; et al. BNT162b vaccines protect rhesus macaques from SARS-CoV-2. Nature 2021, 592, 283–289. [Google Scholar] [CrossRef] [PubMed]
Bahl, K.; Senn, J.J.; Yuzhakov, O.; Bulychev, A.; Brito, L.A.; Hassett, K.J.; Laska, M.E.; Smith, M.; Almarsson, O.; Thompson, J.; et al. Preclinical and Clinical Demonstration of Immunogenicity by mRNA Vaccines against H10N8 and H7N9 Influenza Viruses. Mol. Ther. 2017, 25, 1316–1327. [Google Scholar] [CrossRef] [PubMed]
Bril, F.; Al Diffalha, S.; Dean, M.; Fettig, D.M. Autoimmune hepatitis developing after coronavirus disease 2019 (COVID-19) vaccine: Causality or casualty? J. Hepatol. 2021, 75, 222–224. [Google Scholar] [CrossRef]
Kazazian, H.H., Jr.; Moran, J.V. Mobile DNA in Health and Disease. N. Engl. J. Med. 2017, 377, 361–370. [Google Scholar] [CrossRef] [PubMed]
Coffin, J.M.; Fan, H. The Discovery of Reverse Transcriptase. Annu. Rev. Virol. 2016, 3, 29–51. [Google Scholar] [CrossRef]
Lander, E.S.; Linton, L.M.; Birren, B.; Nusbaum, C.; Zody, M.C.; Baldwin, J.; Devon, K.; Dewar, K.; Doyle, M.; FitzHugh, W.; et al. Initial sequencing and analysis of the human genome. Nature 2001, 409, 860–921. [Google Scholar] [CrossRef]
Ostertag, E.M.; Goodier, J.L.; Zhang, Y.; Kazazian, H.H., Jr. SVA elements are nonautonomous retrotransposons that cause disease in humans. Am. J. Hum. Genet. 2003, 73, 1444–1451. [Google Scholar] [CrossRef]
Hancks, D.C.; Kazazian, H.H., Jr. Active human retrotransposons: Variation and disease. Curr. Opin. Genet. Dev. 2012, 22, 191–203. [Google Scholar] [CrossRef]
Jones, R.B.; Song, H.; Xu, Y.; Garrison, K.E.; Buzdin, A.A.; Anwar, N.; Hunter, D.V.; Mujib, S.; Mihajlovic, V.; Martin, E.; et al. LINE-1 retrotransposable element DNA accumulates in HIV-1-infected cells. J. Virol. 2013, 87, 13307–13320. [Google Scholar] [CrossRef]
Macchietto, M.G.; Langlois, R.A.; Shen, S.S. Virus-induced transposable element expression up-regulation in human and mouse host cells. Life Sci. Alliance 2020, 3, e201900536. [Google Scholar] [CrossRef] [PubMed]
Yin, Y.; Liu, X.Z.; He, X.; Zhou, L.Q. Exogenous Coronavirus Interacts With Endogenous Retrotransposon in Human Cells. Front. Cell Infect. Microbiol. 2021, 11, 609160. [Google Scholar] [CrossRef] [PubMed]
Belancio, V.P.; Roy-Engel, A.M.; Deininger, P. The impact of multiple splice sites in human L1 elements. Gene 2008, 411, 38–45. [Google Scholar] [CrossRef] [PubMed]
Dai, L.; Taylor, M.S.; O’Donnell, K.A.; Boeke, J.D. Poly(A) binding protein C1 is essential for efficient L1 retrotransposition and affects L1 RNP formation. Mol. Cell Biol. 2012, 32, 4323–4336. [Google Scholar] [CrossRef]
Servant, G.; Streva, V.A.; Derbes, R.S.; Wijetunge, M.I.; Neeland, M.; White, T.B.; Belancio, V.P.; Roy-Engel, A.M.; Deininger, P.L. The Nucleotide Excision Repair Pathway Limits L1 Retrotransposition. Genetics 2017, 205, 139–153. [Google Scholar] [CrossRef]
Guo, H.; Chitiprolu, M.; Gagnon, D.; Meng, L.; Perez-Iratxeta, C.; Lagace, D.; Gibbings, D. Autophagy supports genomic stability by degrading retrotransposon RNA. Nat. Commun. 2014, 5, 5276. [Google Scholar] [CrossRef]
Xie, Y.; Mates, L.; Ivics, Z.; Izsvak, Z.; Martin, S.L.; An, W. Cell division promotes efficient retrotransposition in a stable L1 reporter cell line. Mob. DNA 2013, 4, 10. [Google Scholar] [CrossRef]
Shi, X.; Seluanov, A.; Gorbunova, V. Cell divisions are required for L1 retrotransposition. Mol. Cell Biol. 2007, 27, 1264–1270. [Google Scholar] [CrossRef]
Goff, S.P. Host factors exploited by retroviruses. Nat. Rev. Microbiol 2007, 5, 253–263. [Google Scholar] [CrossRef]
Suzuki, Y.; Craigie, R. The road to chromatin—Nuclear entry of retroviruses. Nat. Rev. Microbiol. 2007, 5, 187–196. [Google Scholar] [CrossRef]
Shi, J.; Wang, X.; Lyu, L.; Jiang, H.; Zhu, H.J. Comparison of protein expression between human livers and the hepatic cell lines HepG2, Hep3B, and Huh7 using SWATH and MRM-HR proteomics: Focusing on drug-metabolizing enzymes. Drug Metab. Pharmacokinet. 2018, 33, 133–140. [Google Scholar] [CrossRef] [PubMed]
Kubo, S.; Seleme, M.C.; Soifer, H.S.; Perez, J.L.; Moran, J.V.; Kazazian, H.H., Jr.; Kasahara, N. L1 retrotransposition in nondividing and primary human somatic cells. Proc. Natl. Acad. Sci. USA 2006, 103, 8036–8041. [Google Scholar] [CrossRef] [PubMed]
Macia, A.; Widmann, T.J.; Heras, S.R.; Ayllon, V.; Sanchez, L.; Benkaddour-Boumzaouad, M.; Munoz-Lopez, M.; Rubio, A.; Amador-Cubero, S.; Blanco-Jimenez, E.; et al. Engineered LINE-1 retrotransposition in nondividing human neurons. Genome Res. 2017, 27, 335–348. [Google Scholar] [CrossRef] [PubMed]
*Auteur à qui la correspondance doit être adressée.© 2022 par les auteurs. Détenteur de la licence MDPI, Bâle, Suisse. Cet article est un article en accès libre distribué selon les termes et conditions de la licence Creative Commons Attribution (CC BY) (https://creativecommons.org/licenses/by/4.0/).
Titre de l’article original en anglais : Intracellular Reverse Transcription of Pfizer BioNTech COVID-19 mRNA Vaccine BNT162b2 In Vitro in Human Liver Cell Line
Traduction : Lelibrepenseur.org avec DeepL Translator